細胞を使った毒性試験
細胞を使った毒性試験とは
私たちが日々使う医薬品や化粧品、食品添加物などは、どれも安全性が確認されてから市場に出ています。
その安全性を確認するために行われるのが「毒性試験」です。
従来は実験動物を用いた試験が主流でした。しかし、3R*1の考え方や倫理的観点、迅速性やコストの面などから、近年では「in vitro*2(細胞を主体とした)毒性試験」が広く活用されています。
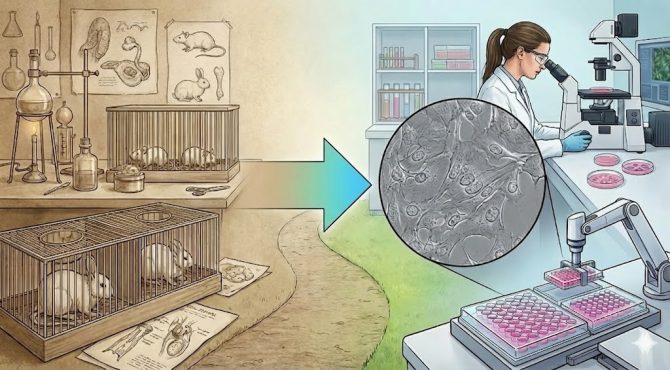
安全性を確認するための毒性試験は実験動物から細胞へ移っています
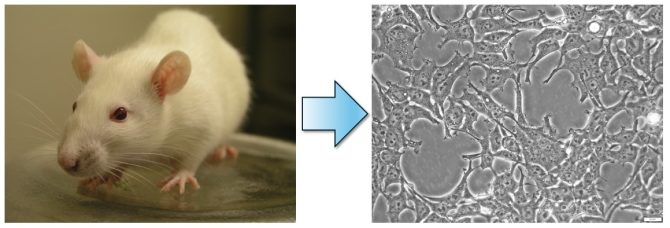
使用される細胞は実験動物由来のものも少なくありません
細胞を培養して、そこに化学物質や素材を加え、その反応を観察することで、人の体にどのような影響を与えるかを評価するのです。
特に皮膚刺激性や細胞へのダメージを調べる試験では、動物ではなくヒト由来の培養細胞を使うケースが増えています。
*1:動物実験における国際的な倫理原則であり、Replacement(代替)・Reduction(削減)・Refinement(改善)の3つの理念を指します。
*2:「イン・ヴィトロ」と発音し、ラテン語で「ガラスの中で」という意味です。生体の外で試験管やディッシュなど人工的な環境でおこなう実験を指します。
細胞毒性試験の主な種類
細胞毒性試験にはいくつかの方法があり、目的や評価したい項目によって使い分けられます。
ATPアッセイ
細胞が生きて活動しているときに作るエネルギー物質「ATP(アデノシン三リン酸)」の量を測定します。
ATPアッセイで利用される反応はルシフェリン・ルシフェラーゼ反応とも呼ばれ、初夏の夜を彩るホタルが持っている発光酵素である「ルシフェラーゼ」を利用することで、細胞中のATPを利用して光を放出させます。
このとき、ATPの量が少ないほど細胞の生存率は低いと、毒性が高いと判断されます。

ホワイトプレートを使用したATPアッセイ
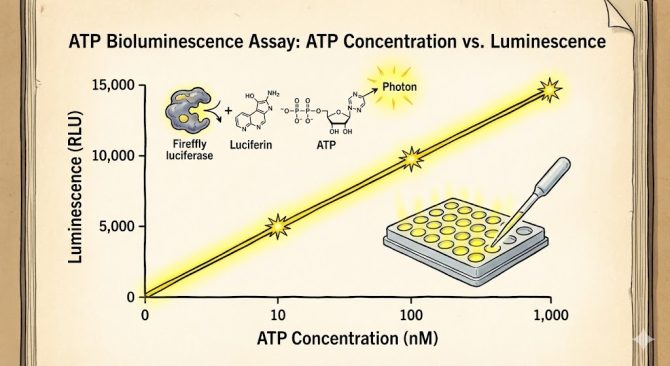
細胞数=ATPが多いほど強く光るので細胞数を推定できます
MTTアッセイ
細胞内にあるミトコンドリアにはエネルギーを作り出すために多くの還元酵素が含まれています。MTT試薬は細胞に取り込まれたあと、これら還元酵素によって紫色のホルマザンに変化し、約570nm*1付近の光をよく吸収するようになります。
これを応用した毒性試験をMTTアッセイと呼び、生きている細胞が多いほど紫色が濃くなるため、細胞の活性度を視覚的に確認できます。
MTTアッセイでは吸光度計などを使用します
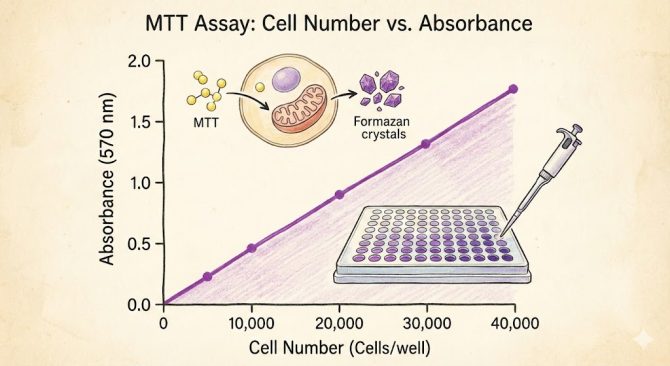
細胞数が多いほど紫色が濃くなるので細胞数を推定できます
*1:日光にはさまざまな波長の光(電磁波)が含まれており、そのうち 約380~750 nm の波長域が可視光線と呼ばれ、人の目には色として認識されます。可視光線は波長によって色が異なり、約570 nm付近の光は黄緑色として知覚されます。
LDHアッセイ
細胞内の細胞質中に存在する乳酸デヒドロゲナーゼ(LDH: Lactate DeHydrogenase)はエネルギーを作り出す「解糖系」の中で機能している酵素で、多くの細胞の中に存在しています。
細胞膜が健全(損傷が無い状況)であれば、この酵素は細胞外へ出ていきませんが、損傷があると細胞外へ漏れ出てしまいますので、その漏れ出たLDHを検出することで毒性を評価することができます。
実際にはLDHそのものを直接検出しているのではなく、LDHが触媒する反応(乳酸からピルビン酸への酸化反応)によって生成される電子を受け取った分子(NADHとよばれる低分子化合物の一種)を介した発色や発光反応のシグナル量を測定しています。

LDHアッセイでも吸光度計などを使用します
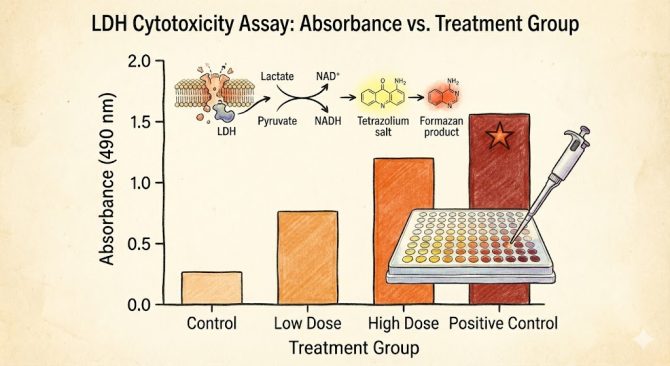
ダメージを受けた細胞が多いほど色が濃くなるため毒性を評価することができます
コロニーアッセイ
細胞がもつ増殖能および長期生存能を評価する方法として用いられる手法です。
この試験では、単一の細胞が分裂を繰り返し、コロニー(集落)を形成できるかどうかを指標として細胞の生存性を評価します。
健全な細胞であれば、細胞分裂を繰り返して数十から数百個の細胞からなるコロニーを形成しますが、化学物質、放射線、薬剤などによる損傷を受けると、細胞は分裂能力を失い、コロニーを形成できなくなります。
そのため、形成されたコロニーの数や大きさを評価することで、細胞に与えられた毒性や増殖阻害効果を定量的に解析することが可能です。
実際の評価では、処理後に一定期間培養した細胞を固定・染色し、目視または画像解析によってコロニー数をカウントします。
このアッセイでは、短時間の代謝活性を測定するATPアッセイやLDHアッセイとは異なり、「生き残った細胞が将来的に増殖できるか」という長期的な細胞生存性を反映する点が大きな特徴です。

細胞を増殖させた後に特殊な溶液で細胞を染色します
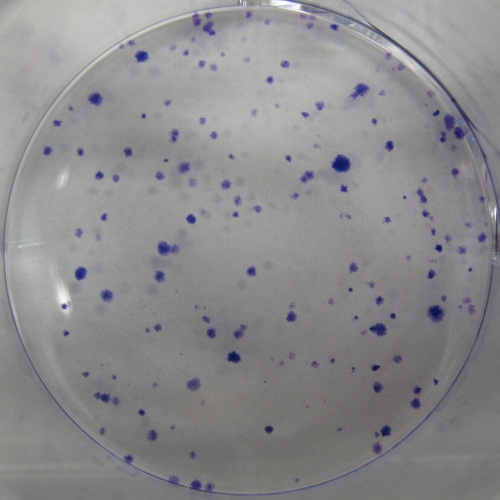
染色された細胞のコロニーを計数することで毒性を評価します
他にも遺伝的な変異(遺伝毒性)を及ぼすかどうかを評価する「染色体異常試験」や「細胞小核試験」などがあります。
これらの試験を組み合わせることで、化学物質がもつ細胞への毒性を評価することができます。
試験に使用される細胞モデル
細胞毒性試験で用いられる細胞は、評価の目的や想定される暴露臓器(直接接触することで影響が及ぶ臓器)、作用機序に応じて選択されます。
例えば、皮膚刺激性や皮膚腐食性を評価する場合には、皮膚角化細胞(ケラチノサイト)やヒト再構築皮膚モデルが用いられます。
肝臓での代謝や肝毒性を評価する場合には、肝細胞(ヘパトサイト)や肝臓由来細胞株が使用されます。
細胞の増殖性や長期生存能を調べる場合には、線維芽細胞や上皮系細胞株が用いられ、コロニーアッセイなどにより増殖能の低下や分裂阻害が評価されます。
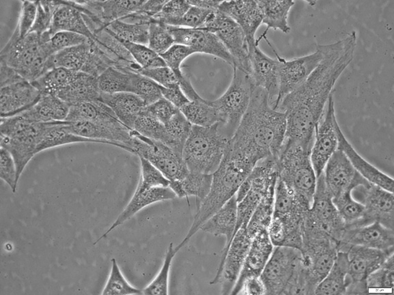
線維芽細胞の一例
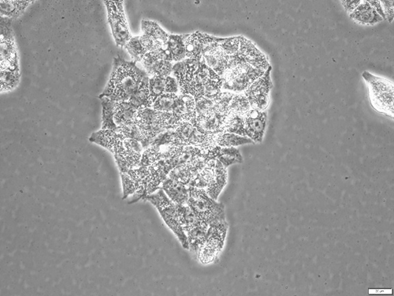
肝細胞の一例
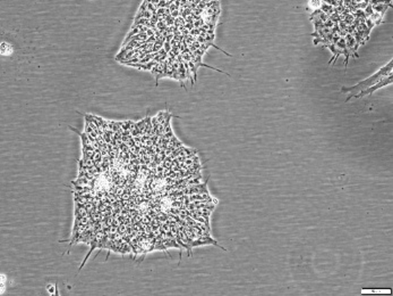
多分化能を持つiPS細胞
これらの試験では、ヒト由来の細胞株だけでなく、マウス、ラット、ハムスターなどの動物由来細胞株が使用されることもあり、試験目的や既存データとの整合性に応じて選択されます(例:V79、CHO、L929細胞など)。
近年では、再生医療や創薬研究の進展に伴い、iPS細胞やES細胞から分化誘導した機能性細胞も使用される場合があります。
さらにそれらから構成される三次元(3D)培養やスフェロイド、オルガノイドといった、より生体に近い構造・機能を再現した培養系を用いた毒性評価の構築も進んでおり、これら新しい培養スタイルは、従来の培養では評価が困難であった臓器特異的毒性や慢性毒性の予測精度向上に寄与すると期待されています。
マウスエンブリオアッセイ(MEA)とは
MEA(Mouse Embryo Assay:マウスエンブリオアッセイ)は、マウスの受精卵を使って、培地や実験器具、添加物などに含まれる微量の有害物質の影響を調べる試験です。
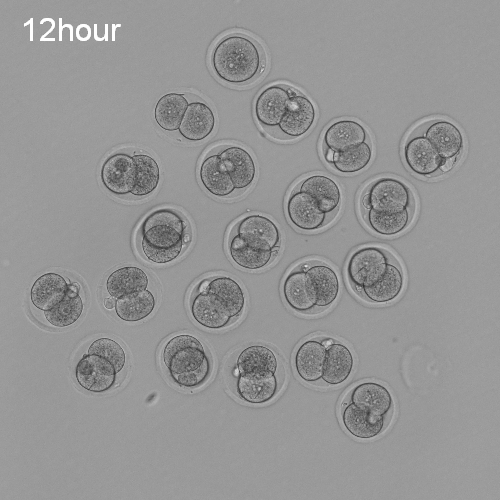
マウス前核期胚を培養して12時間後の状態
ほとんどが2細胞期胚となっている
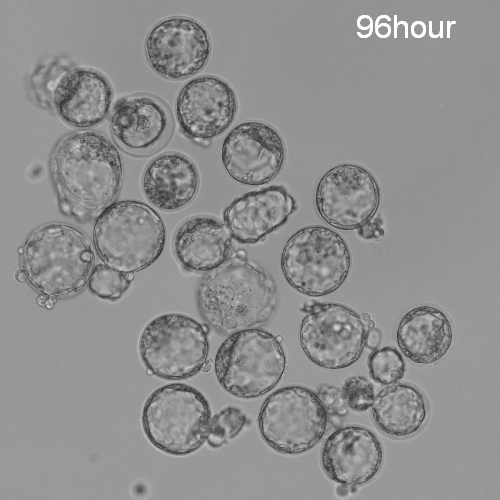
MEAでは指定時間内に胚盤胞期へ移行できた胚の数を計数します
マウスの胚はとても繊細で、わずかな毒性物質でも成長が阻害されてしまいます。
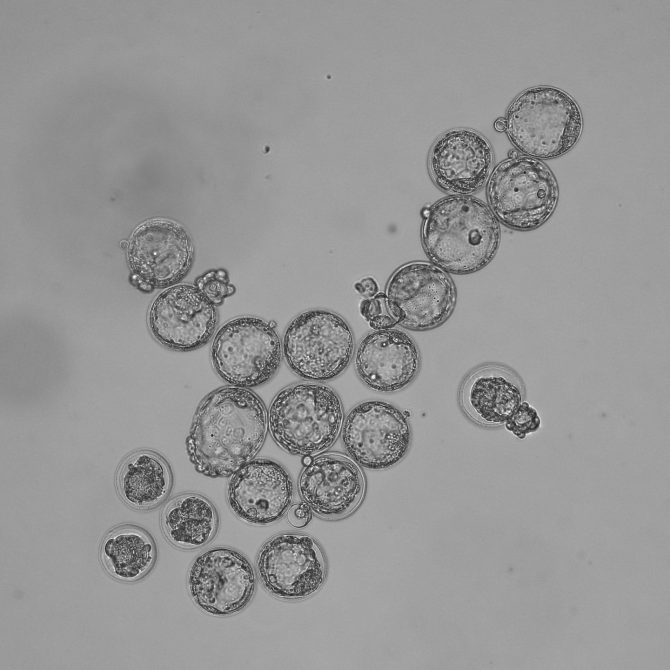
胚盤胞形成率85.7%(21個中18個が胚盤胞期胚)のためMEAでは合格判定
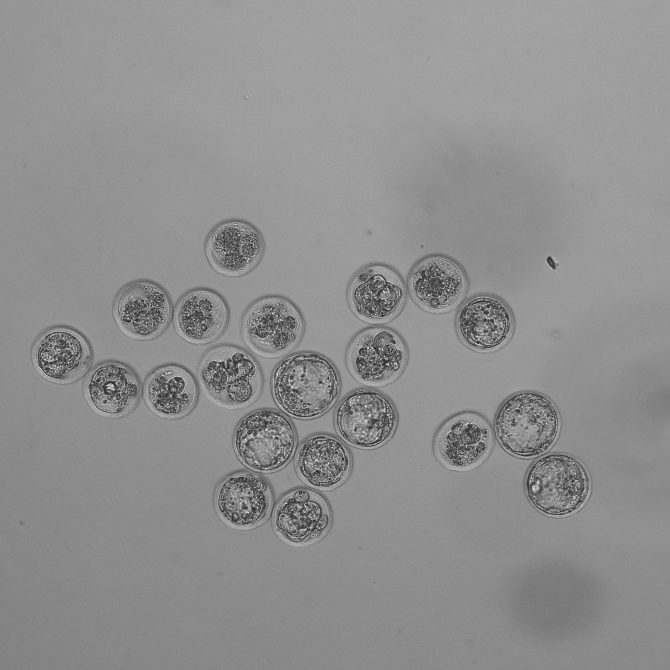
胚盤胞形成率42.9%(21個中9個が胚盤胞期胚)のためMEAでは不合格判定
この試験は、生殖医療や不妊治療の分野で、胚培養に使う環境の安全性を確認するうえで欠かせません。
そのため、MEAで良好な結果*1が得られた製品は「高い安全性を持つ」と判断できます。
培地やディッシュ・プレートといった培養容器など細胞が直接触れる製品はもちろんのこと、近年では培養に関する製品の安全性を示すために、実際に培養している環境を評価する用途にも用いられています。

インキュベーター内の加湿水に設置して抗菌作用を示す製品の安全性評価

加湿水は培地蒸発を防ぐ重要な役割があります
*1:大部分の細胞培養関連製品は指定された時間(前核期胚では96時間後・2細胞期胚では72時間後)に、胚盤胞に到達した胚の数が播種した胚の80%以上であることを指標としており、米国FDA(食品医薬品安全局)でのガイダンス*2に記載されています。
*2:米国FDAサイト内のMEAガイドライン参照:According to the FDA guidance Mouse Embryo Assay for Assisted Reproduction Technology Devices… (FDA, 2021).
各分野での応用事例
細胞を使った毒性試験は、さまざまな分野で役立っています。
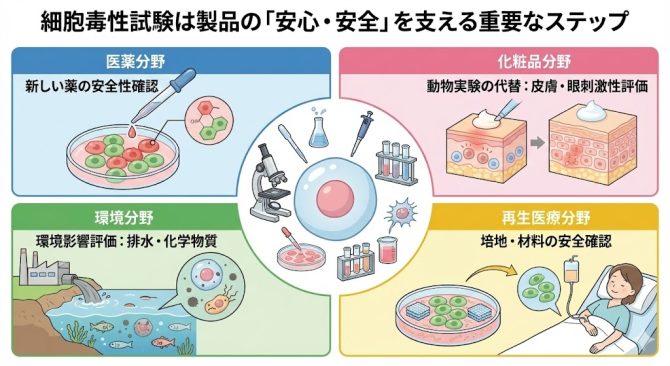
私たちが安心・安全な生活を送るために細胞毒性試験は重要な役割を果たしています
- 医薬分野:新しい薬の候補化合物の安全性確認に利用される。
- 化粧品分野:皮膚刺激性や眼刺激性の評価に、動物実験の代替として使用される。
- 環境分野:排水や化学物質が環境に与える影響を評価する。
- 再生医療分野:細胞培養用の培地や材料の安全確認に不可欠。
このように、細胞毒性試験は製品の「安心・安全」を支える重要なステップとなっています。
国際的な動向と規制
国際的には、OECD(経済協力開発機構:Organisation for Economic Co-operation and Development)が策定する「試験ガイドライン(OECD Test Guidlines)」に基づいて毒性評価が行われています。
これらのガイドラインはデータ相互受け入れ(MAD:Mutual Acceptance of Data)の原則の下で運用されており、各国間で試験結果の信頼性や再現性を確保する役割を担っています。
また、EUのREACH規則(化学品の登録・評価・認可および制限に関する規則:Registration, Evaluation, Authorisation and Restriction of Chemicals)では、化学物質の安全性データを提出する際に、「できる限り動物実験を避ける」ことが求められており、動物実験は最終手段と位置付けられています。
そのためin vitro試験を始めとする非動物試験法の活用が強く求められています。
こうした背景から、細胞を用いた非動物試験法の需要は、今後ますます高まると考えられます。
毒性試験の課題と今後の展望
従来の細胞試験は、平面上で細胞を培養する「2D培養」が主流でした。
しかし、これは実際の体内環境とは異なるという課題があります。
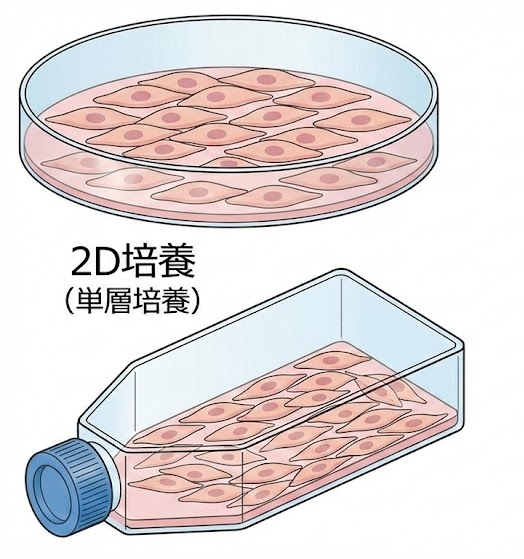
ディッシュやTフラスコでの細胞は平面的に増殖します
体内で立体的な構造を持つ臓器を完全に再現できません
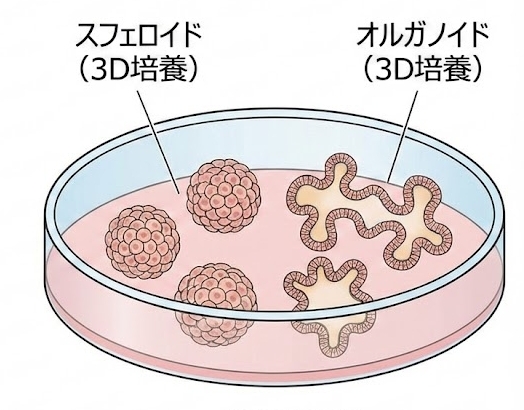
適切な条件にすることで立体的に培養することが可能です
体内の臓器に近い機能を持たせることができます
最近では、細胞を立体的に培養する「3D培養」や、微小流体技術を使った「Organ-on-a-Chip(臓器チップ)」の研究が進んでいます。特に後者は2010年に発表された「Lung(肺)-on-a-Chip」を皮切りに、様々な臓器の機能を模倣したチップ*1が開発されました。現在では、これらを連結してヒトの全身機能や臓器間の連携(コミュニケーション)まで再現する「Body-on-a-Chip」の開発*2が世界中で進んでいます。
このように生体機能をチップ上で再現したシステムを「生体模倣システム(MPS:Microphysiological Systems)」と呼びます。日本でも、日本医療研究開発機構(AMED:Japan Agency for Medical Research and Development)が主導するプロジェクト*3として、活発に研究が進められています。
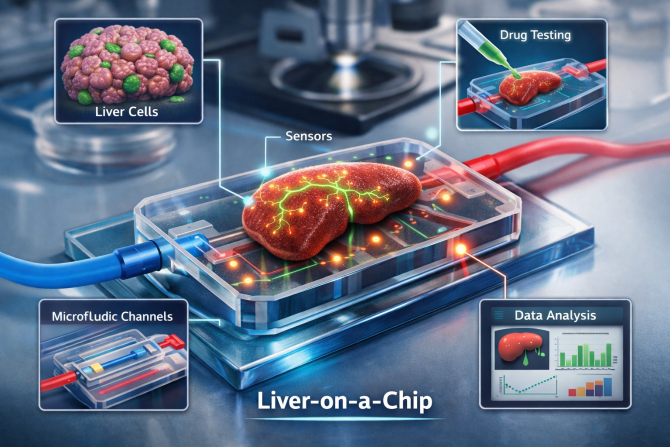
肝臓の臓器チップ(イメージ図)
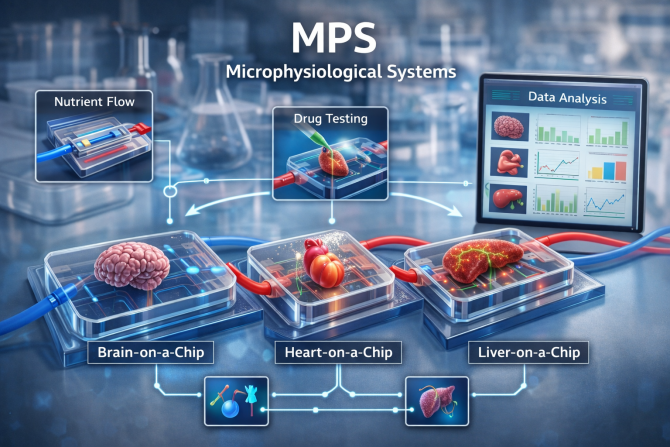
生体模倣システム(イメージ図)
MPSの最大の利点は、実験動物では見抜けなかったデータを効率よく収集できる点です。特に、「動物には無害だが、ヒトには重篤な副作用が出る」というリスクを未然に防ぐ手段として期待されています。
その典型例が、1950年代に発売された睡眠・鎮痛剤による薬害事件です。この薬はマウスやラットでは毒性がほぼ見られませんでしたが、ヒトの胎児に対しては極めて高い毒性を示しました。これは動物とヒトの「種差(しゅさ)」が原因でしたが、当時の動物実験では見抜くことができませんでした。この悲劇を教訓に、「ヒトの細胞」を用いた毒性評価が強く求められるようになり、現在のMPS開発へとつながっています。
これにより、臓器間の相互作用や血流の影響まで再現でき、より精度の高い毒性評価が期待されています。
*1:Huh D, et al. Reconstituting organ-level lung functions on a chip. Science. 2010;328(5986):1662-1668.
*2:Ma C, et al. Organ-on-a-Chip: A New Paradigm for Drug Development. Trends Pharmacol Sci. 2021 Feb;42(2):119-133.
*3:日本医療研究開発機構 再生・細胞医療・遺伝子治療プロジェクト 再生医療・遺伝子治療の産業化に向けた基盤技術開発事業(再生医療技術を応用した高度な創薬支援ツール技術開発)
安全性の高い製品を選ぶために
毒性試験で高評価を得た培地や器材を選ぶことで、より安全で信頼性の高い実験ができます。
特に細胞や胚を扱う実験では、わずかな成分の違いが結果に大きく影響することがあります。
そのため、試験実績が明確で信頼できるメーカーの製品を選ぶことが大切です。
まとめ
細胞を使った毒性試験は、単に「安全性を確認するための検査」ではなく、私たちがより安心して研究を進めるための基盤技術といえます。
ATP測定による細胞毒性試験や、マウスエンブリオアッセイのような精密な評価を通じて、製品の品質と安全性が保証されることで、細胞培養や不妊治療など、さまざまな分野の信頼性が支えられています。
研究の確実性を高めるためにも、毒性試験で高評価を得た安全性の高い製品を選ぶことが、信頼できる成果を生む第一歩です。