その混合、大丈夫ですか?培養に関係する試薬に潜む危険性
細胞培養の現場では、日々さまざまな試薬を扱います。
培地、添加剤、洗浄液、消毒剤など、ひとつひとつは「いつものもの」であっても、組み合わせや使い方を誤ることで、予期せぬ化学反応や有害物質の発生を引き起こす可能性があります。
その結果、培養中の細胞だけでなく作業者であるヒトの健康や安全にも影響を及ぼす危険性が潜んでいます。

混ぜると危険性が高まる化学物質は細胞培養の現場にも存在します。
今回は、細胞培養に関わる方であれば一度は意識しておきたい「混合によるリスク」について、具体例を交えながら考えてみたいと思います。
日常操作の中に潜む「つい」の落とし穴
細胞培養は、丁寧なルーティンワークの積み重ねです。
その一方で、
- 「pHが少しズレたから調整しよう」
- 「使い終わった廃液は、とりあえず消毒しておこう」
といった判断を、深く考えずに行ってしまう場面も少なくありません。
この「つい」が、思わぬトラブルにつながることがあります。
① pH調整による浸透圧上昇のリスク
~試薬調製での注意点(NaOHとHClなどの入れ過ぎにご用心)~
細胞培養に関連する試薬を調製する際には、溶液のpH(酸性・アルカリ性の度合い)を調整する操作が必要になる場面が多くあります。
たとえば、接着細胞を培養容器から剥離するために用いられる EDTA 溶液はアルカリ性条件でなければ十分に溶解せず、細胞接着性を高めるコーティング剤として利用される コラーゲン溶液は酸性条件下で安定に溶解します。
このため、実験の現場では NaOH(アルカリ)や HCl(酸)を添加して pH を調整する操作が日常的に行われています。
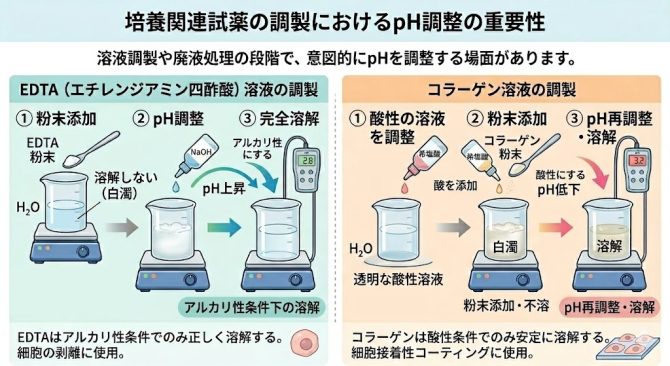
溶液作製の段階ではpH調整のためHClやNaOHなどを添加します。
しかしここで注意すべき点があります。
pHを合わせるためにNaOHやHClを大量に加えると、溶液中には ナトリウムイオン(Na⁺)や塩化物イオン(Cl⁻)といったイオンが増加します。これらは水中では「塩(えん)」として存在するため、結果として溶液中の塩濃度が上昇します。
塩濃度が上昇すると、溶液の浸透圧も上昇します。
細胞は周囲の浸透圧が大きく変化するとストレスを受けやすく、わずかな変化でも培養結果に影響する可能性があります。
これまでの研究では、培地の浸透圧が400mOsmを上回ると細胞死を導く遺伝子が活性化される傾向にあることが知られています*1。
またMSC(間葉系間質細胞*2)を用いた実験では、塩濃度の過剰な上昇によって浸透圧が変動した場合、細胞増殖や形態に悪影響が生じることが報告されています*3。
このことからも、pH 調整に伴う過剰な塩濃度の上昇は避けるべきであると言えます。
~培養中での培地のpH調整~
また培養をおこなっている現場では、培地のpHが想定よりも酸性やアルカリ性に傾く場合があります。たとえば細胞が増殖し過ぎた場合や、(あまり考えたくないですが)微生物によるコンタミネーションが発生した時*4などでは酸性に大きく傾き、培地成分の分解が進行した場合ではアンモニアが発生することでアルカリ性に傾くこともあります。
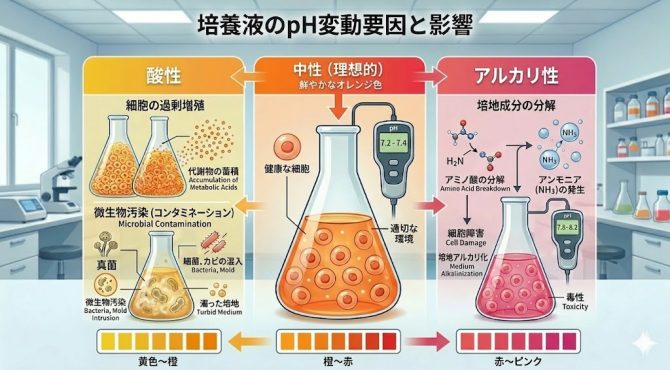
培地(培養液)のpHは様々な要因で変動します。
そのため、商業的に抗体やタンパク質などを生産するために細胞を大量培養する場合、たとえばバイオリアクター(培養タンク)を用いた培養では、pHセンサーで培地のpHを常時測定し、pHが低下した場合にはアルカリ(NaOHなど)を、pHが上昇した場合には酸(HClなど)を添加して 自動的にpHを制御するシステムが用いられることがあります。
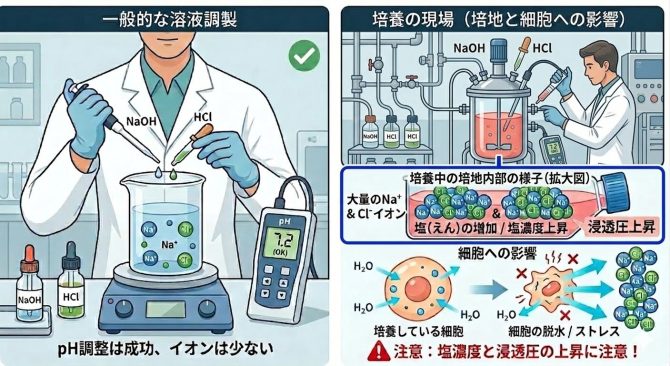
細胞を培養している時には無理にpHを調整しない方が賢明です。
ただし、このような場合でも 酸や塩基の添加量が多すぎると培地の浸透圧が上昇し、細胞の増殖や生存率に影響する可能性が指摘されています。そのため、大規模培養では酸・アルカリの不要な添加は避けるなど、慎重な制御が行われます。
このことからも、pH調整に伴う過剰な塩濃度の上昇は避けるべきであると言えます。
なお、一般的な実験室スケールの培養(10cmディッシュやTフラスコなど)では、培養中の培地にNaOHやHClを直接加えてpHを調整することはあまり一般的ではありません。
これは、細胞培養用の培地には炭酸水素ナトリウム(NaHCO₃)が含まれており、インキュベーター内のCO₂(通常5%程度)と平衡を保つことで緩衝系(バッファー)として働き、培地のpHをある程度安定に保つ仕組みになっているためです。
この炭酸水素ナトリウムとCO₂ガスによる緩衝系(重炭酸緩衝系)によって、細胞の代謝などによって多少の酸(H+)やアルカリ(OH–)の量が増えても、急激なpH変動は起こりにくくなっています。
*1:Malek AM, et al. Mannitol at clinical concentrations activates multiple signaling pathways and induces apoptosis in endothelial cells. Stroke. 1998;29(12):2631-2640.
*2:従来は間葉系幹細胞と呼ばれていましたが、2025年5月より間葉系間質細胞と呼称することとなりました。
*3:Zhang H, et al,. Effects of Changes in Osmolarity on the Biological Activity of Human Normal Nucleus Pulposus Mesenchymal Stem Cells. Stem Cells Int. 2022 Apr 23;2022:1121064.
*4:Segeritz CP, Vallier L. Cell Culture: Growing Cells as Model Systems In Vitro. Basic Science Methods for Clinical Researchers. 2017:151–72.
② 漂白剤とアルコールの危険な組み合わせ
消毒の定番である漂白剤(次亜塩素酸ナトリウム)とエタノール。
どちらもラボでは頻繁に使われますが、この2つが混ざるとハロホルム反応によりクロロホルムが発生する可能性があります。
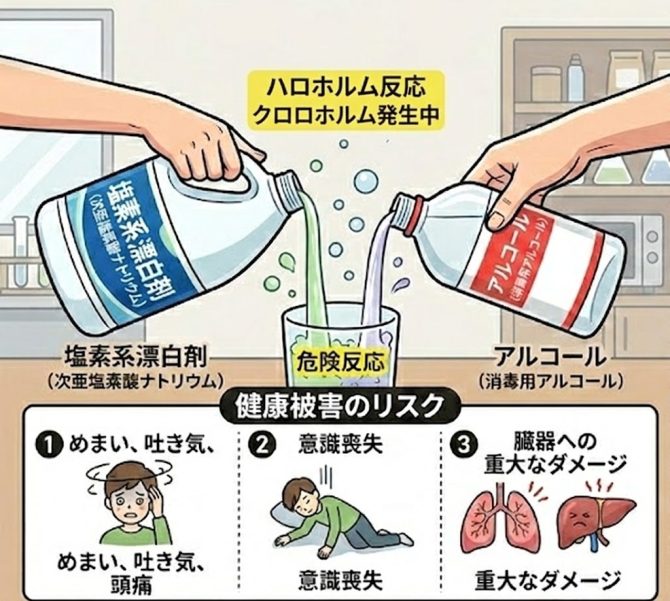
漂白剤とアルコールを混ぜるとクロロホルム発生の危険性が高まります。
クロロホルムは揮発性が高く、吸入すると中枢神経抑制や肝障害などの健康被害を引き起こす有害物質です。
例えば、
- インキュベーターやクリーンベンチ内にエタノールを吹き付けた後、漂白剤を染み込ませたペーパーで吹き上げる。
- 廃液容器にアルコールを加えて、さらに漂白剤を投入する。
といったケースで条件がそろえば、発生リスクはゼロではありません。
③ 漂白剤とRNA抽出試薬の混合がもたらす深刻な危険
RNAやDNAなど核酸の抽出で使われるグアニジン塩酸塩などの試薬は、強い変性作用を持つためタンパク質を可溶化する(水に溶けやすくする)ため、遺伝子を取り扱う実験でよく使われています。
その一方で、このグアニジン塩酸塩は漂白剤と混合すると非常に危険です。

核酸抽出実験で良く使われる試薬は絶対に塩素系漂白剤と混合しないでください。
この組み合わせでは、
- 人体にとって有毒なガス(例. HCN:シアン化水素・青酸)が発生する可能性
- 副次的に爆発性のあるガス(例. NCl3:トリクロラミン)が発生する可能性
が指摘されています。
いずれも少量であっても人体や周囲環境に深刻な影響を及ぼすガスですので、大学や教育機関によっては注意書きが用意されています*1, 2。
特に密閉性の高い実験室や排水管内で発生した場合、気づかないうちに被曝するリスクがありますので、絶対に混合しないようにしてください。
*1:アメリカ カリフォルニア州のスタンフォード大学・環境保健安全部が公開するファクトシート(注意書き)
*2:アメリカ ミネソタ州のセントオラフ大学・化学物質衛生/実験室安全部門が公開する安全ガイドライン
④抗生物質の安易な併用による細胞培養への影響
ペニシリンやストレプトマイシンなどの抗生物質は、細胞培養におけるコンタミネーションへの対策として広く使用されています。
これらは混合溶液として市販されており、英語では「Pen/Strep」や「P/S」と表記されることがあり、培養の現場では「ペンスト」や「ペニスト」と呼ばれることもあります。
培地中の濃度としては、ペニシリンが100[U/mL]、ストレプトマイシンが100[μg/mL]が最もよく利用されています。
なお、ペニシリンの濃度はmgやgといった質量ではなく、細菌の増殖を抑える効き目を示すU(ユニット)という単位で表されます。
しかし、複数の抗生物質の併用や高濃度・長期添加は、標的である細菌だけでなく培養細胞にも影響を及ぼす可能性があります。
特にストレプトマイシンなどのアミノグリコシド系抗生物質は、細菌が持つリボソームの働き(タンパク質を合成していく反応)を阻害する薬剤*1ですが、動物細胞が持っているミトコンドリアは進化的には細菌に由来すると考えられている(細胞内共生説)ため、ミトコンドリアでのタンパク質合成に影響を与える可能性が指摘されています。
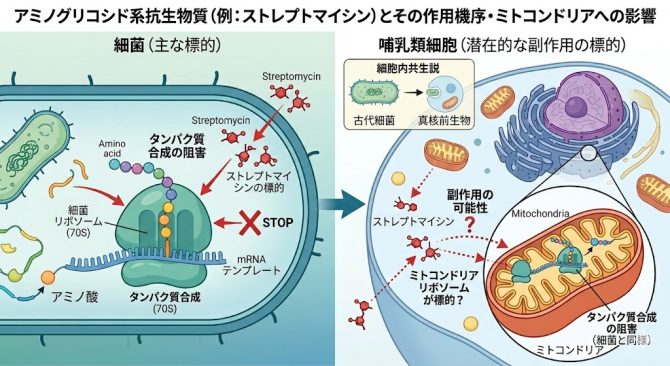
アミノグリコシド系抗生物質は細菌が持つリボソームに作用します
しかしミトコンドリアの中にあるリボソームにも影響を及ぼす可能性があります。
その結果として、
- ミトコンドリア機能の低下*3
- ATP生産量の減少*4
- 細胞増殖の遅延*5
- 遺伝子発現への影響*6
などが報告されています。
また、抗生物質は細胞種によって感受性が異なり、特にiPS細胞をはじめとする幹細胞を培養する際や薬物代謝解析をおこなう場合には、培地に抗生物質を添加せずに培養することが多々あります*7。
そのため抗生物質はあくまで補助的手段であり、基本は無菌操作の徹底です。常用する場合でも、最小有効濃度での使用と、必要性の定期的な再評価が重要です。
*1:細菌を始めとする原核生物が持つリボソームと、ヒトや動物などの真核生物が持つリボソームは構造が異なるため、アミノグリコシド系抗生物質は細菌に良く効くとされています*2。
*2:Recht MI, et al. Basis for prokaryotic specificity of action of aminoglycoside antibiotics. EMBO J. 1999;18(11):3133-3138.
*3:O’Reilly M, et al. Gentamicin Affects the Bioenergetics of Isolated Mitochondria and Collapses the Mitochondrial Membrane Potential in Cochlear Sensory Hair Cells. Front Cell Neurosci. 2019;13:416. Published 2019 Sep 13.
*4:Hong S, et al. Evidence That Antibiotics Bind to Human Mitochondrial Ribosomal RNA Has Implications for Aminoglycoside Toxicity. J Biol Chem. 2015 Jul 31;290(31):19273-86.
*5:Stefano GB, et al. Antibiotics May Trigger Mitochondrial Dysfunction Inducing Psychiatric Disorders. Med Sci Monit. 2017 Jan 7;23:101-106.
*6:Suárez-Rivero JM, et al. Mitochondria and Antibiotics: For Good or for Evil? Biomolecules. 2021 Jul 17;11(7):1050.
*7:厚生労働省の「ヒト(自己)iPS(様)細胞加工医薬品等の品質および安全性の確保について(2025年1月17日一部改正)」において「抗生物質は細胞培養系で極力使用しないことが望まれている」や「抗生物質に頼るのではなく、高度な無菌操作や設備によって(微生物による)汚染を防ぐべき」という記述があります。
⑤ 排水管や廃液タンク内で起こる「気づきにくい混合」
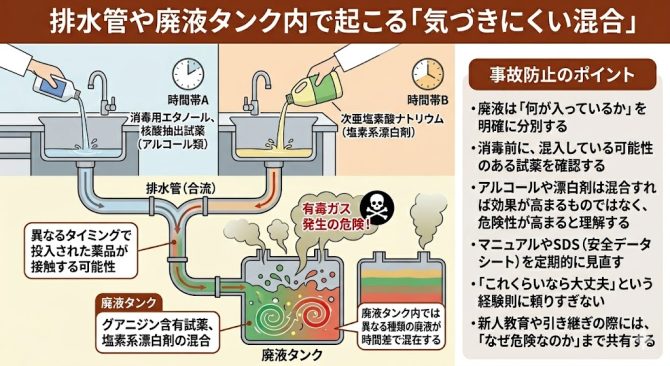
目に見えない・気づきにくい混合にも注意しましょう。
実験室内で特に見落とされがちなのが、排水管や廃液タンク内での化学物質の混合です。
別々のシンクに流した場合や、異なるタイミングで廃液タンクに投入した場合でも、排水配管の途中やタンク内で薬品が接触する可能性があります。
特に注意が必要なのは、
- 消毒や核酸抽出などで使用したエタノールなどのアルコール類
- 次亜塩素酸ナトリウムなどを含む塩素系漂白剤
- 核酸抽出やタンパク質グアニジン塩酸塩系の試薬
このような危険な混合を防ぐため、実験を行う施設ごとに定められている廃液処理のルールや分別方法を事前によく確認し、それに従った廃液処理を徹底することが重要です。
実際に、グアニジン含有試薬と漂白剤の混合により有毒ガスが発生した事例については、大学の環境安全部門などが注意喚起しています*1。
重要なのは「同時に混ぜていないから安全」という考え方では不十分であることです。
排水系統は実験室内で合流しており、また廃液タンク内では異なる種類の廃液が時間差で混在する可能性があります。
したがって、廃液は化学的性質や反応性を事前に確認した上で適切に分別し、必要に応じて用途別・種類別に廃液タンクを分けて管理することが重要です。
特に反応性のある廃液同士が混合しないよう、タンク内容物の表示や運用ルールを明確化して運用することが求められます。
具体的には以下のような点です。
- 廃液は「何が入っているか」を明確に分別する
- 消毒前に、混入している可能性のある試薬を確認する
- アルコールや漂白剤は混合すれば効果が高まるものではなく、危険性が高まると理解する
- マニュアルやSDS(安全データシート)を定期的に見直す
- 「これくらいなら大丈夫」という経験則に頼りすぎない
特に新人教育や引き継ぎの際には、「なぜ危険なのか」まで共有することが、事故防止につながります。
おわりに
ここで取り上げた事例に共通するのは、危険な試薬を扱っているという意識が薄れた場面で事故が起きているという点です。
細胞培養で日常的に使用する試薬の多くは、単体では大きな問題を起こしません。
しかし、その濃度や状態(ガスやミストなど)、また排水経路などでの混合といった様々な条件が重なることで、はじめてリスクが目に見えるようになります。
特に廃液処理や清掃など、実験終了後の工程は注意が緩みやすく、見落としが生じやすい領域です。
さらに、こうした影響は必ずしも重大事故として現れるとは限りません。
顕微鏡観察やPCRといった様々な工程を経て初めて確認できる細胞ダメージや再現性の低下、作業者の体調不良といった形で表面化することもあります。
だからこそ重要なのは、「何が混ざり得るのか」「それはどこで起こり得るのか」を常に意識することです。
日々の操作を見直し、「その混合は本当に安全か」と問い直す姿勢で常に作業にのぞみ、細胞の品質と実験環境、そして作業者の安全を守りましょう。