【コンタミ】細胞培養を脅かす2つの存在
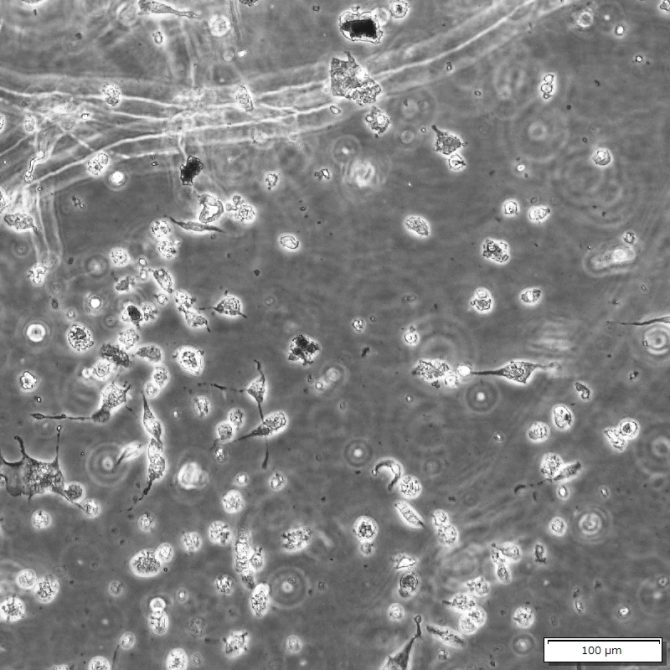
あれ?細胞の様子が変です。死んだ細胞が多いですし
糸状のものが無数に浮かんでいます…まさか!!

やっぱり…微生物による汚染が起こっていました…
おそらく真菌(カビ)のコンタミネーションです
細胞培養の現場で絶対に避けなければならないことが「コンタミネーション(汚染)」です。
以前の記事でも簡単にご紹介しましたが、今回はより詳しくご説明いたします。
参考:【コンタミ】細胞培養を襲う脅威
このコンタミネーション(以降コンタミと表記)に対する理解が深まるにつれ、おこなうべき対策がより洗練されていき、結果として細胞培養と向き合う姿勢も自然と変わっていきます。
ここでは、実際の現場でよく遭遇するコンタミについて
【①微生物によるコンタミ】
と
【②クロスコンタミ(交差汚染)】
の2つに分類し、それらの発生原因や確認方法のほか、発生時の対処についてご説明します。
【①微生物によるコンタミ】
最も頻繁に起こり、最もダメージの大きいコンタミの原因がこちらです。
特に細菌・真菌・酵母やマイコプラズマといった微生物の侵入が多く、ほとんどが無菌操作の小さな油断から発生します。
ここではコンタミ発生時の状況や特徴を、微生物別に説明します。
細菌(Bacteria)によるコンタミでは何が起こるのか?

細菌によるコンタミネーションとは
原因となる微生物(一部)
・Bacillus(バチルス属 例:納豆菌)
・Lactobacilllus(ラクトバチルス属 例:乳酸菌)
・Staphylococcus(スタフィロコッカス属 例:ブドウ球菌)
・Pseudomonas(シュードモナス属 例:緑膿菌)
・Escherichia(エシェリヒア属 例:大腸菌)
コンタミ発生時の状況と特徴
・数時間~1日以内に培地が白濁する。増殖速度は後述の真菌や酵母と比べると圧倒的に早い。
・pHが急激に低下する(フェノールレッド入り培地では黄色化)。
・pHが徐々に上昇する(フェノールレッド入り培地ではピンク~赤紫色化)。
・培地から異臭が放たれる。
・顕微鏡下では無数のドット上の物体が存在し、移動する様子も確認される。
・芽胞(エンドスポア)*1を形成することで厳しい環境でも生存可能な状態となる場合がある。
・細胞の増殖は著しく抑制され、全滅の危険性がある。
・ペニシリンやストレプトマイシンといった抗生物質は細菌の増殖を抑えることができる。
原因となる微生物は日常に身近なものが多いため、これによるコンタミの発生確率が高い傾向にあります。
私たちが普段食べることのある納豆はバチルス属の細菌による発酵であり、チーズやヨーグルトはラクトバチルス属の細菌による発酵です。
納豆菌に代表されるバチルス属の微生物は、豆類などに含まれるタンパク質を分解してアミノ酸とアンモニアを作り出すプロテアーゼを分泌します。バチルス属に限らず、多くの細菌や(後述する)一部の真菌はプロテアーゼを分泌することでアンモニアを産生することがあり、その結果、培地のpHがアルカリ性に傾く場合があります。
一方、乳酸菌に代表されるラクトバチルス属の微生物は牛乳などの中にある糖を代謝することで大量の「乳酸」を作り出します。そのため、ラクトバチルス属が培地で増殖すると大量の乳酸が作り出され、結果として培地のpHが酸性に傾いてしまいます。
このように、培地のpHが酸性に傾くか、アルカリ性に傾くかは、増殖した微生物がどのような代謝産物を生成するかによって決定されます。
しかし、培地pHがどのように変わっていたのか?を考察する以前に重要なのは、コンタミネーションが確認された時点で、汚染源となったディッシュやTフラスコを速やかに除去し、オートクレーブ滅菌や殺菌・消毒処理などにより二次的な汚染を防止することです。
また、細菌によるコンタミネーションへの予防として抗生物質の添加は有効ですが、耐性菌が出現する可能性があります。
さらにiPS細胞やMSC、初代培養細胞などでは、増殖や分化、遺伝子発現*3に影響を及ぼすことがあり、実験結果の信頼性を損なう恐れがあります。このため、抗生物質の使用には十分な注意が必要です。
*1:芽胞(エンドスポア)とは一部の細菌が作ることができる極めて頑丈な細胞構造です。消毒剤や熱、乾燥に対して非常に高い抵抗性を示すため、しばしば食中毒を引き起こす原因となります(例:夏場に置きやすい作り置きカレーで起こりやすい。再度加熱してもセレウス菌やウェルシュ菌の芽胞が残るため食中毒を引き起こす*2)。
*2:田中啓子ら. 惣菜中のセレウス菌芽胞の制御における加熱処理の効果. 食品衛生学雑誌. 2005;46(1):1-7.
*3:Skubis A, et al. Impact of Antibiotics on the Proliferation and Differentiation of Human Adipose-Derived Mesenchymal Stem Cells. Int J Mol Sci. 2017 Nov 24;18(12):2522.
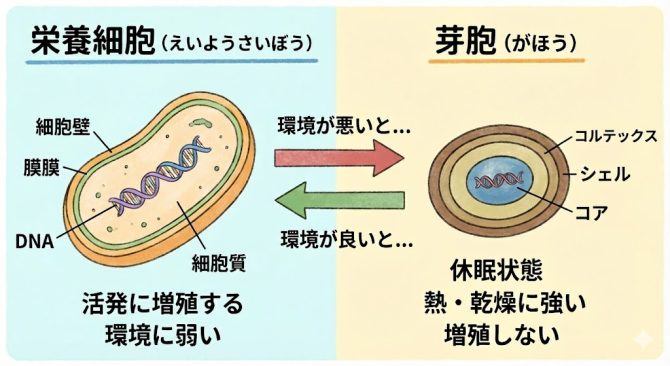
一部の細菌は非常に頑丈な芽胞を作ります
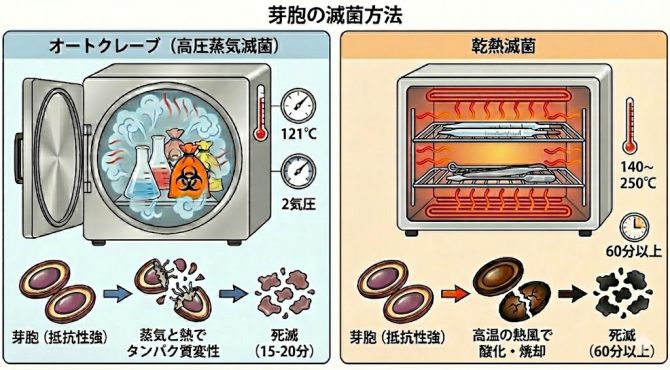
芽胞はオートクレーブや乾熱滅菌で死滅できます
真菌(Fungi)いわゆるカビによるコンタミでは何が起こるのか?

真菌(カビ)によるコンタミとは?
原因となる微生物(一部)
・Aspergillus(アスペルギルス属 例:こうじカビ)
・Penicillium(ペニシリウム属 例:アオカビ)
・Cladosporium(クラドスポリウム属 例:黒カビ)
コンタミ発生時の状況と特徴
・数日以内に培地が白濁し、さらに培地表面や内部に綿毛状の物体が浮遊する。増殖速度は酵母や細菌と比べると遅い。
・物体の色は白色・緑色・青色・黒色など様々。
・多くの場合はpHが低下(乳酸や酢酸など有機酸といった酸性物質の分泌が活発であることが多い)、または上昇。
・培地から異臭が放たれる。
・顕微鏡下では細長い菌糸が縦横無尽に伸びている様子が確認される。
・環境変化により強いストレスを受けると胞子(スポア)を作り出すことがある。
・胞子(スポア)を形成する場合、その胞子がインキュベーター内の気流に乗ることで被害を拡大する恐れがある。
・細胞の増殖は著しく抑制され、全滅の危険性がある。
・ペニシリンやストレプトマイシンといった抗生物質がほとんど効かない。
細菌と同じく日常に身近なものが多いため、コンタミの発生確率が高い傾向にあります。
カマンベールチーズやブルーチーズ、鰹節などは熟成工程でカビを用いますので、これらを飲食したときには注意が必要です。
またエアコンの送風口で見かける黒っぽいシミは黒カビであることが多く、そこを通過した空気はコンタミを引き起こすリスクを高めます。
こういったカビが培地に混入し増殖すると、乳酸やクエン酸、酢酸といった有機酸を始めとする酸性物質が大量に分泌(あるいは分泌された酵素が菌体外で有機酸を形成)されるため、多くの場合は培地のpHは酸性に傾きます。
しかしプロテアーゼを始めとしたアンモニア生産に関わる物質も存在するため、培地のpHがアルカリ性に傾くこともあります。
なお、いわゆる抗生物質はカビ(真菌)にほとんど効きませんのでご注意ください。
というのも、抗生物質の代表格であるペニシリンは「細菌特有の細胞壁の合成を妨害する」、ストレプトマイシンは「細菌などの原核生物*1のタンパク質合成を妨害する」といったメカニズムで細菌の増殖を防ぎます。
カビ(真菌)の細胞壁はキチン・マンナンなどの多糖類に脂質が混じったものであり細菌とは全く異なっています。またカビ(真菌)は真核生物*2でありタンパク質合成の手順が細菌と異なっています。こういったことから抗生物質のターゲットのほとんどが細菌にあり、カビ(真菌)には効力を示しません(あるいは効力が弱くなる)ので注意が必要です*3。
またカビ(真菌)は菌糸を伸ばして成長・増殖します(栄養菌糸の状態)が、栄養が少ない状況(例えばプラスチックやステンレス表面など栄養が少ない環境)では環境変化に強い胞子(スポア)を作り出すことがあります。
この胞子は非常に軽いため気流に乗りやすく、インキュベーター庫内を循環する気流に乗ってしまうと、庫内全体に胞子が行き渡ることとなるので汚染が拡大します。
そのため、カビと思われるものを発見したら、胞子を形成して被害が広がる前に速やかに処置することが必要です。

あの白いモヤモヤは…カビ?
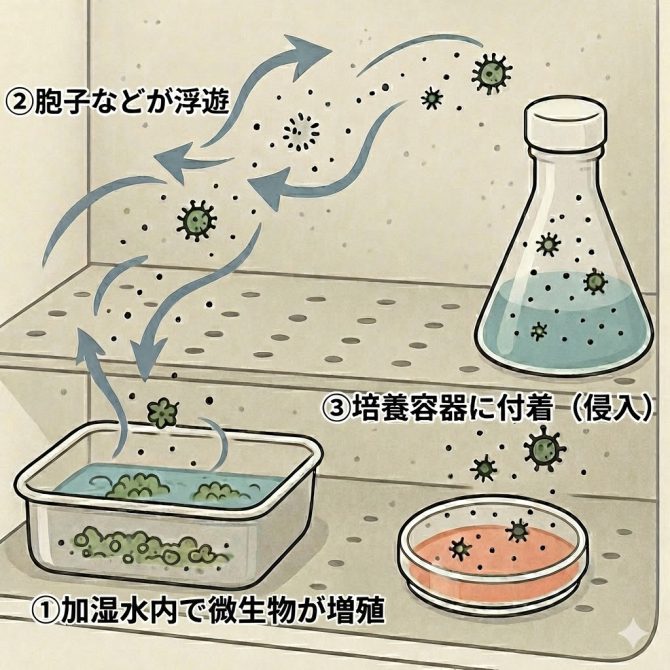
胞子による被害が広がる前に対処をしましょう!
*1:原核生物とは細胞核を持たず遺伝子(DNAやRNA)がそのままの状態で細胞内に存在する生物です。大腸菌や納豆菌といった細菌などが原核生物です。
*2:真核生物とは細胞核という構造体の中に遺伝子が存在する生物です。カビや酵母といった微生物の他にも私たち人間や多くの動物が真核生物です。
*3:真菌に効果を示す抗生物質は存在しますが(アムホテリシンBなど)、培養している細胞にも影響を及ぼすので使用には注意が必要です。
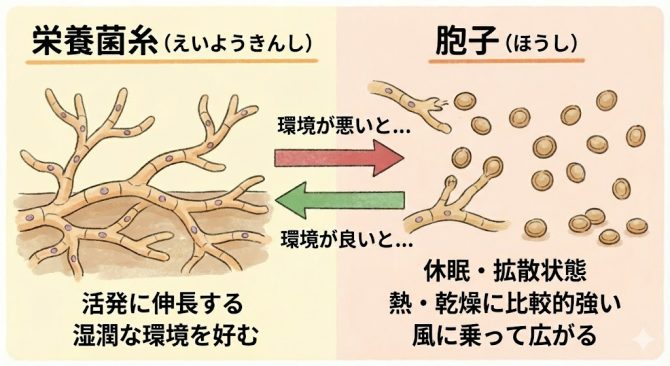
真菌(カビ)は環境に応じて胞子を作り出します
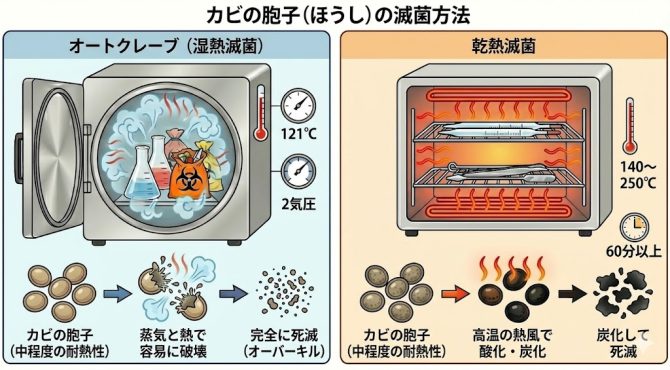
胞子はオートクレーブや乾熱滅菌で死滅できます
真菌の一種である酵母(Yeast)によるコンタミでは何が起こるのか?
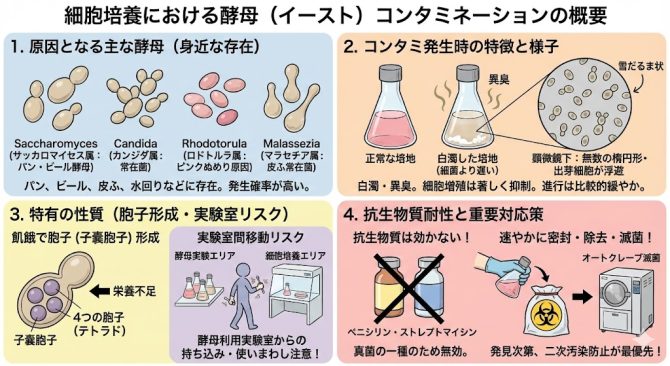
酵母によるコンタミとは?
原因となる微生物(一部)
・Saccharomyces(サッカロマイセス属 例:パン酵母やビール酵母)
・Candida(カンジダ属 例:カンジダ症の原因)
・Rhodotorula(ロドトルラ属 例:水回りのピンクぬめりの原因)
・Malassezia(マラセチア属 例:皮ふの常在菌)
コンタミ発生時の状況と特徴
・細菌と比べると進行が遅い傾向にある。
・培地は白濁することが多い。
・培地のpHは変動するものの細菌や真菌と比べると緩やかな傾向にある。
・培地から異臭が放たれる。
・環境次第、特に飢餓状態では胞子(子嚢胞子)を作り出す。
・顕微鏡下では無数の楕円形構造体が浮遊している様子が確認される。
・細胞の増殖は著しく抑制され、全滅の危険性がある。
・ペニシリンやストレプトマイシンといった抗生物質がほとんど効かない。
酵母もまたこれまでの細菌や真菌と同じく、生活に身近なものが多いため、コンタミの原因となりやすい傾向にあります。
細菌や真菌のときと同様、培地に混入・増殖した場合はpH変動や異臭発生が引き起こされます。
また酵母は真菌の一種であるため、真菌と同じく抗生物質がほぼ効かない傾向にあります。
こういった酵母は遺伝子の研究やタンパク質の相互作用の研究*1で頻繁に利用されることもあり、酵母を利用している実験室への行き来や実験器具の使いまわしなどには注意が必要です。
また、酵母は通常、出芽によって分裂し増殖しますが、環境が悪化すると子嚢(しのう)胞子を作り出します。
真菌(カビ)の胞子と異なり、サイズが大きいため空気中に拡散することはほぼありませんので、庫内の他のフラスコやディッシュへの汚染拡大のリスクは真菌(カビ)よりも低いものの、細菌や真菌の時と同様、コンタミが確認された時点で、汚染源となったディッシュやTフラスコを速やかに除去し、ピペットや器具の使いまわしなどによる二次汚染を防止することが重要です。
*1:ツーハイブリッド法と呼ばれる遺伝子発現を利用したタンパク質の相互作用(くっつくかどうかの判定)が代表的です。また2016年ノーベル生理学賞・医学賞に輝いたオートファジー(自食作用)も酵母を利用した研究から生まれました*2。
*2:Ohsumi Y. Molecular mechanism of autophagy in yeast, Saccharomyces cerevisiae. Philos Trans R Soc Lond B Biol Sci. 1999 Sep 29;354(1389):1577-80; discussion 1580-1.
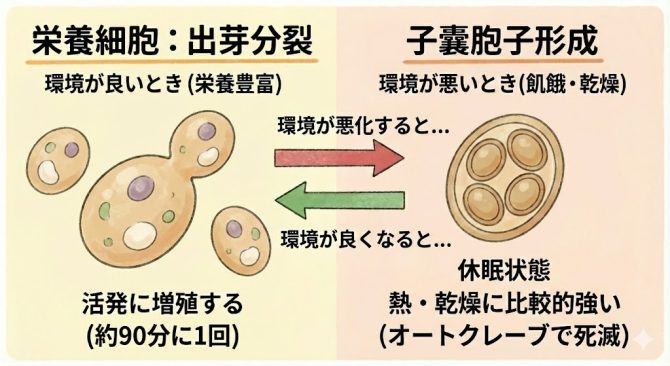
酵母も環境によっては胞子(子嚢胞子)をつくります
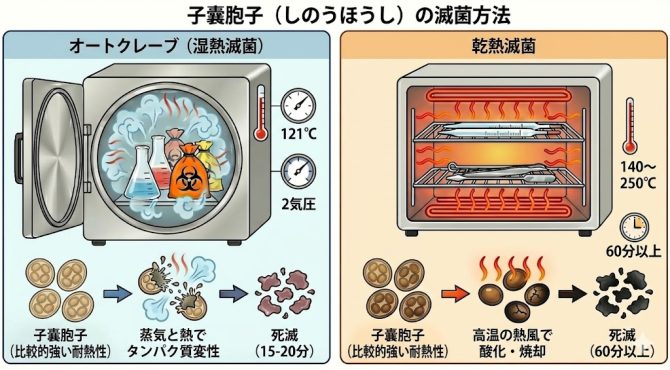
子嚢胞子もオートクレーブや乾熱滅菌で死滅できます
マイコプラズマ(Mycoplasma)によるコンタミでは何が起こるのか?
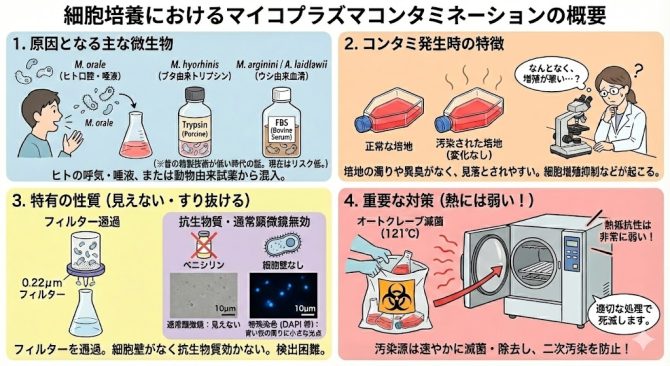
マイコプラズマによるコンタミとは?
原因となる微生物(一部)
・Mycoplasma orale(マイコプラズマ・オラレ…ヒト口腔常在菌であるため呼気や唾液にも含まれる)
・Mycoplasma hyorhinis(マイコプラズマ・ヒオリニス…酵素「トリプシン」を豚から得る際の精製技術が低い時代に混入していた)
・Mycoplasma arginini(マイコプラズマ・アルギニニ…培地に添加する「血清」を牛から得る際の精製技術が低い時代に混入していた)
・Acholeplasma laidlawii(アコレプラズマ・レイドラウィー…同上)
コンタミ発生時の状況と特徴
・汚染が発生しても培地に変化がほとんど現れず、異臭も発しないことが多いため見落とされやすい。
・細胞の増殖抑制や膜組成の変化を始めとする様々な影響が発生する。
・通常の顕微鏡下では大きな変化が見られない。
・マイコプラズマは細胞壁を持たず、タンパク質合成が細菌とは異なるため抗生物質がほとんど効かない。
・直径0.2~0.3μmであるため、通常の濾過滅菌で使用する0.22μmフィルターを通過してしまう。
・検出にはVero細胞などに感染後での核染色(Vero細胞の細胞核以外に無数の小さな核が視認される)の他、PCRによる検出が使われる。
細菌や真菌、酵母などと異なり、培地の色変化や異臭といった目立つような変化が起きません。
「なんとなく、細胞の増殖が悪いような気がする…」
そう思って検査をおこなったら、知らないうちにマイコプラズマに感染していた、ということがあります。このことから
過去、投稿された論文中に使われた細胞の中で、そのいくつかがマイコプラズマ汚染していたことが報告されています*1。
マイコプラズマの検査方法には、Vero細胞やNIH/3T3細胞などの宿主細胞に疑わしい培地を加えて数日培養し、Hoechst 33342 や DAPI で染色する方法があります。感染している場合、宿主細胞核とは別に微小な点状のDNAシグナルが観察されます。
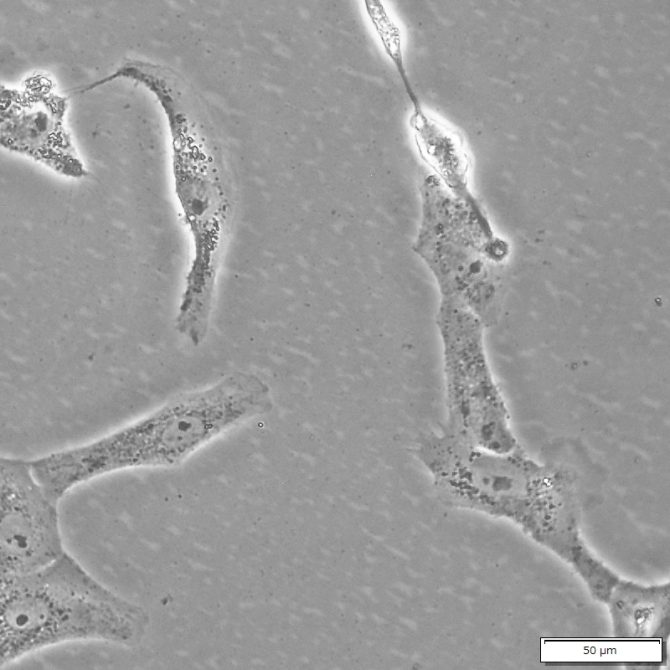
宿主細胞(Vero細胞)
※マイコプラズマ感染していません
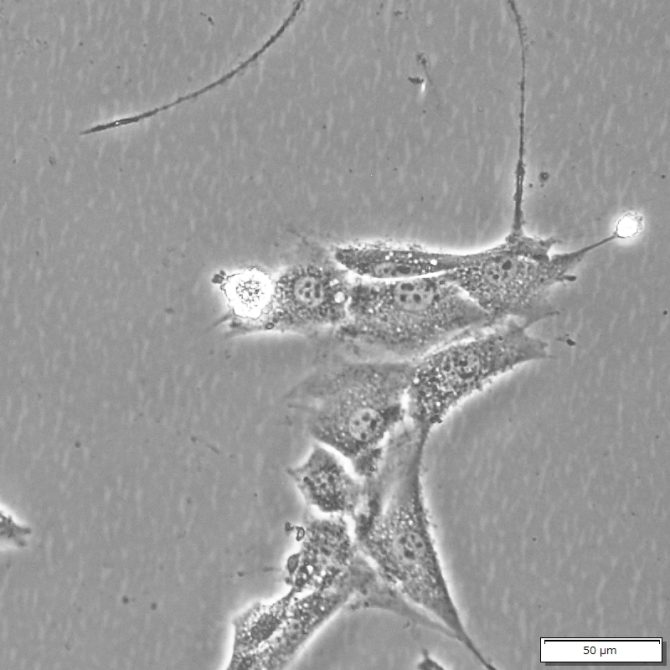
宿主細胞(NIH/3T3細胞)
※マイコプラズマ感染していません
もう一つの方法として、PCRによりマイコプラズマ特有の遺伝子配列をDNAレベルで検出する方法があり、簡便で感度が高いため現在はこちらが主に用いられています。

PCRをおこなう
サーマルサイクラー

PCR反応溶液の作製

PCR反応中

PCR結果を判定中
(電気泳動)
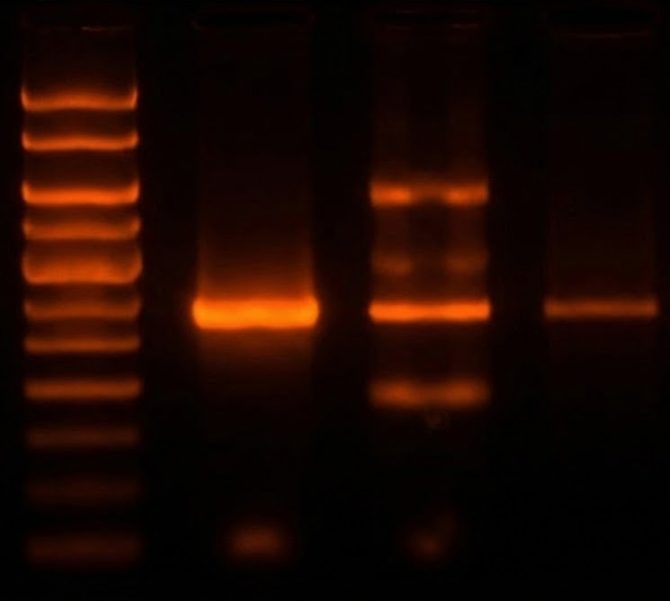
PCR結果
(DNAの蛍光染色)
なお、マイコプラズマは非常に小さく(長径1~2μm、短径0.1~0.2μmで繊維状)、通常のフィルターろ過滅菌(孔径0.22μm)では除去されません。一方、熱に対する抵抗性は胞子や芽胞と比べて非常に弱いことから、オートクレーブや乾熱滅菌などで処理をおこなうことで汚染源となったディッシュやTフラスコを速やかに除去し、二次汚染を防止することが重要です。
微生物によるコンタミの原因7選
肉眼では確認できない微生物の混入(コンタミネーション)は、些細な操作ミスや環境の不備から発生します。リスクを最小限に抑えるため、特に以下の7項目に注意して細胞培養をおこないましょう。
~作業者や培養操作に関連する原因~
(1) 作業者の発する飛沫・落下菌(最大の汚染源)
クリーンベンチ内での会話、咳、くしゃみによる飛沫や、作業者の皮膚・髪の毛・衣類から落下するホコリが培地に混入します。
これらは細菌や真菌だけでなく、厄介なマイコプラズマ汚染の主要な原因となります。マスクの正しい着用と、操作中の私語厳禁が基本です。
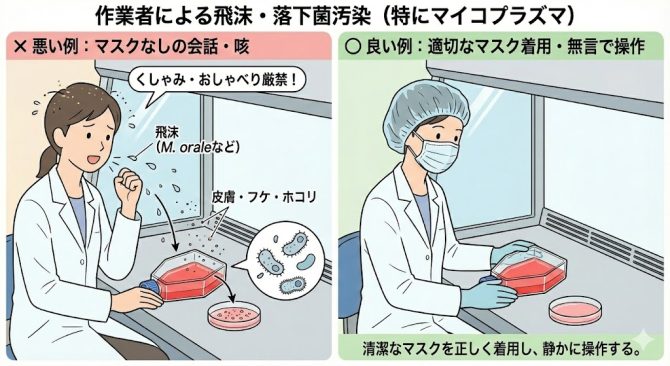
会話やくしゃみ、咳をした際の飛沫の中には微生物が潜んでいるかもしれません

マスクや手袋を装着して飛沫や落下菌を防ぎましょう

場合によってはクリーンスーツを着用することも有効です
(2) 無菌操作の不徹底
滅菌されたピペットの先端、培地ボトルの口、フラスコの内側などに、作業者の手袋や衣類の袖、未滅菌の器具が誤って接触することで菌が付着します。「清潔なもの」と「不潔なもの」の境界線を常に意識する動作が必要です。
また、作業中は手袋表面に付着した微生物が落下する可能性があるため、フタを開けたままのディッシュやボトルの上を手指が通過しないよう注意しましょう。
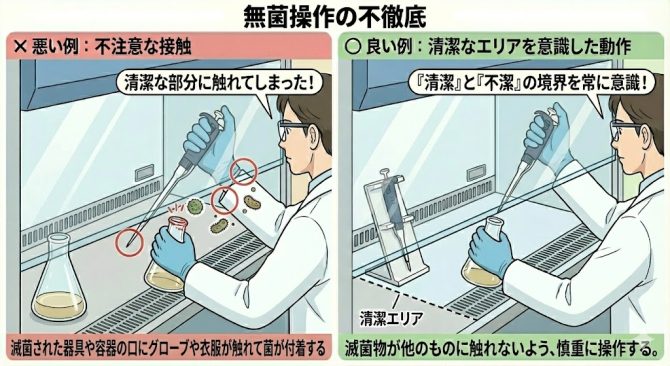
何が清潔で不潔なのかを常に意識して作業しましょう

フタと手指の位置に気を付けましょう

ピペットの取扱いに注意しましょう
~培養環境や機器に関連する原因~
(3) クリーンベンチ内の気流妨害
クリーンベンチの吸気口(グリル)の上に物を置いたり、ディッシュやフラスコなどの器具を詰め込みすぎたりしていませんか?
正常なエアカーテン(層流)が乱れると、培養操作をおこなうためのワークスペース内の無菌環境が保てなくなります。
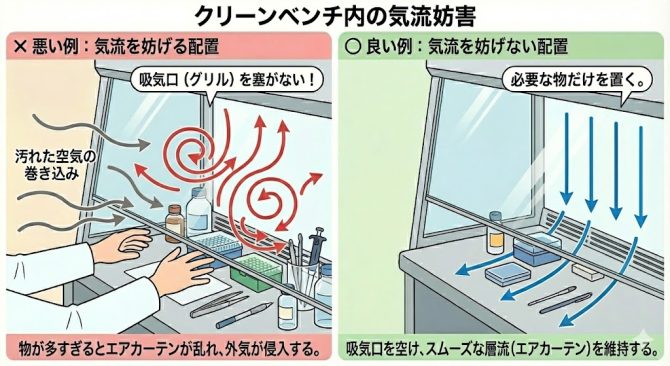
培養操作の無菌環境を維持することが重要です

クリーンベンチの中は常に整理しておきましょう

空気取り込み口を塞がないようにしましょう
(4) インキュベーター内の加湿水の汚染
インキュベーター庫内の湿度を保つための加湿バットの水は温かいため、カビや細菌の格好の温床となります。
ここで増殖した微生物(特に真菌・カビの胞子)が庫内を流れる気流に乗ることで、フラスコの隙間から侵入する可能性があります。
そのため定期的な加湿水(超純水・RO水をオートクレーブやフィルターろ過滅菌したもの)の交換と清掃が不可欠です。
また加湿水からの汚染を防ぐため銀イオンを活用した抗カビ製品などの活用も効果的です。
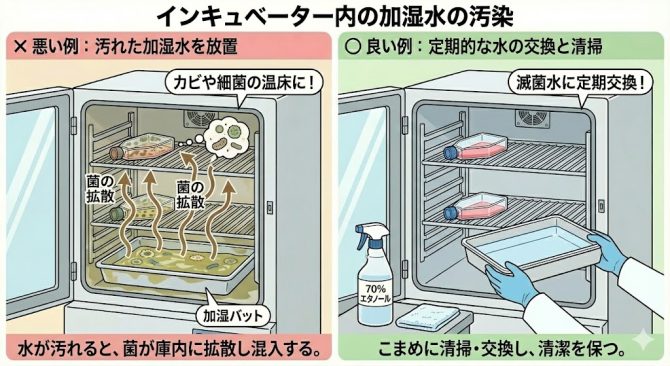
微生物の温床となる加湿水はしっかりと管理しましょう

加湿水には滅菌水を使用しましょう

銀イオンによる抗カビ製品を利用しましょう
加えて、庫内を循環する空気中の微粒子を捕集する専用フィルターを装着することで、インキュベーター内全体の微生物汚染リスクを大幅に低減することが可能となります。

理想的なインキュベーター庫内(イメージ図)
加湿水に銀イオンを活用した抗カビ製品+微粒子捕集フィルターを装着
(5) インキュベーターの設置状況
※現場レベルで意外に見落とされるポイント
インキュベーターを設置している部屋の温度を一定に保つため、ほとんどの場合、エアコン(空調設備)が設けられています。
こういった空調設備が洗い場の近くにある場合、空調からの気流によって目に見えない水しぶきや汚れ、微生物を含むエアロゾルが拡散する可能性があります。
こうした気流がインキュベーター付近に到達すると、扉の開閉時に周囲の浮遊微生物が庫内へ流入し、コンタミネーションのリスクを高める要因となりえます。
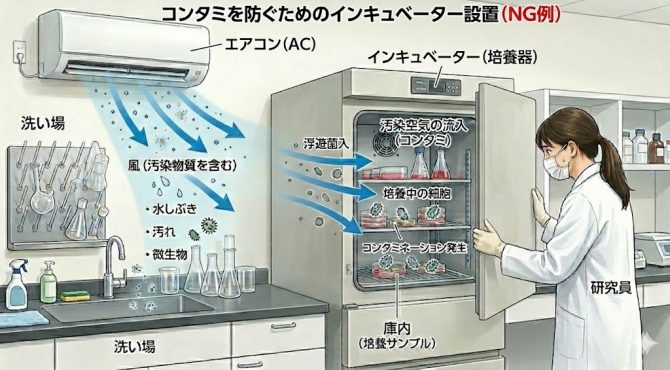
目に見えにくい「空気の動線」にまで気を配ることも重要です
エアコン(空調設備)からの気流そのものに加え、その気流がどこを通るかという「空気の動線」にまで気を配ることも重要です。
同様に、人や物の往来が多い出入口付近では、部屋の外気の流入や乱流の発生によりホコリや浮遊微生物の濃度が高まることも考えられますので、ここも設置環境としては望ましくありません。
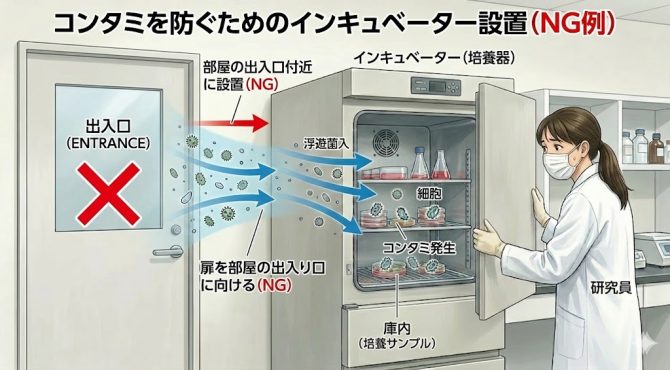
空気の動線が乱れやすい出入口付近にインキュベーターを設置することは推奨できません
(6) 恒温水槽(ウォーターバス)からの持ち込み
培地を温める目的で使用する恒温水槽の温水が汚染されている場合、培地ボトルの外側やキャップのネジ山に、微生物を含んだ水滴が付着することがあります。これらの水滴を十分に拭き取らないまま、あるいは消毒用アルコールなどによる適切な表面消毒を行わずにクリーンベンチへ持ち込むことは、作業エリア全体を汚染する大きな原因となります。
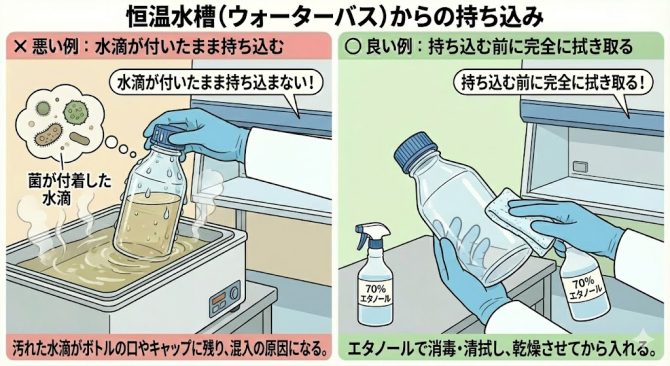
培地や洗浄液など加温にはくれぐれも注意してください
(施設によってはアルコールの使用を制限している場合があります)

恒温水層の水は常に清潔な状態を保ちましょう!

恒温水層の水はしっかりと拭き取りましょう!
(7) 液体窒素の液相での保存
細胞などのサンプルを長期凍結保存する液体窒素タンクには、「液相保存」と「気相保存」があります。
液相保存では、クライオチューブが液体窒素に直接浸かるため、万一液体窒素中に微生物を含むホコリなどが混入している場合、それらがチューブ表面に付着する可能性があります。またチューブに微細な破損があると、解凍時に汚染物が内部へ侵入するリスクも否定できません。
一方、気相保存ではサンプルは液体窒素の蒸気層で冷却されるため、液体との直接接触がほとんどありません。このため、交差汚染のリスク低減という観点からは、気相保存がより安全な方法として推奨されています。
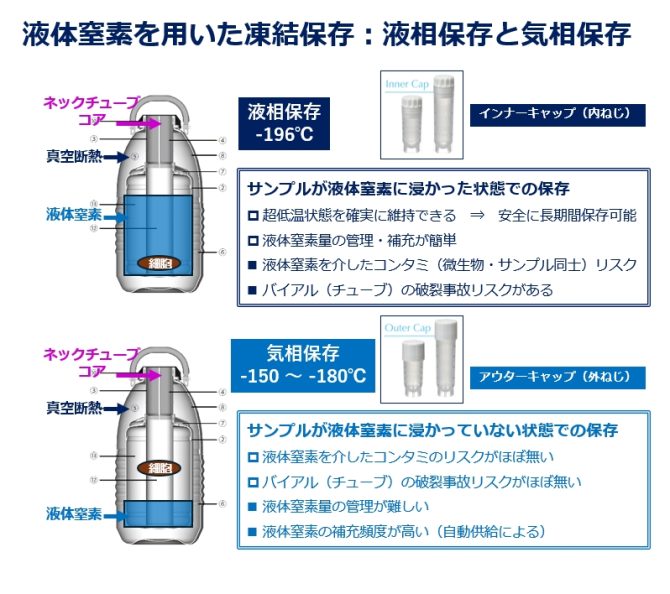
液相保存と気相保存の特徴と違い
実際に液相保存が原因でコンタミの事故が報告された例は極めて少なくリスクは低いとされています*1。
しかしFDA(米国所品医薬品局)では、細胞や組織の保存において液相(Liquid Phase)保存よりも気相(Vapor Phase)保存を強く推奨している一文*2が見受けられていることから、気相保存を選択する施設が増えつつあります。
*1:Bajerski F, et al. Microbial occurrence in liquid nitrogen storage tanks: a challenge for cryobanking?. Appl Microbiol Biotechnol. 2021;105(20):7635-7650.
*2:FDAの細胞バンク取扱いに関するガイダンス「Characterization and Qualification of Cell Substrates and Other Biological Materials Used in the Production of Viral Vaccines for Infectious Disease」中の10ページ目(pdfでは13枚目)
【②クロスコンタミネーション】
ここまでは「微生物によるコンタミ」についてお話ししてきました。
コンタミにはもう一つの種類があり、それが「クロスコンタミネーション(交差汚染。以降、クロスコンタミと表記)」と呼ばれるもので、「ある細胞を培養している中に、別の種類の細胞が混ざってしまうこと」を指します。
(例:肝臓の細胞を培養していたはずなのに、いつの間にか増殖の速い別の細胞に乗っ取られていた、など)
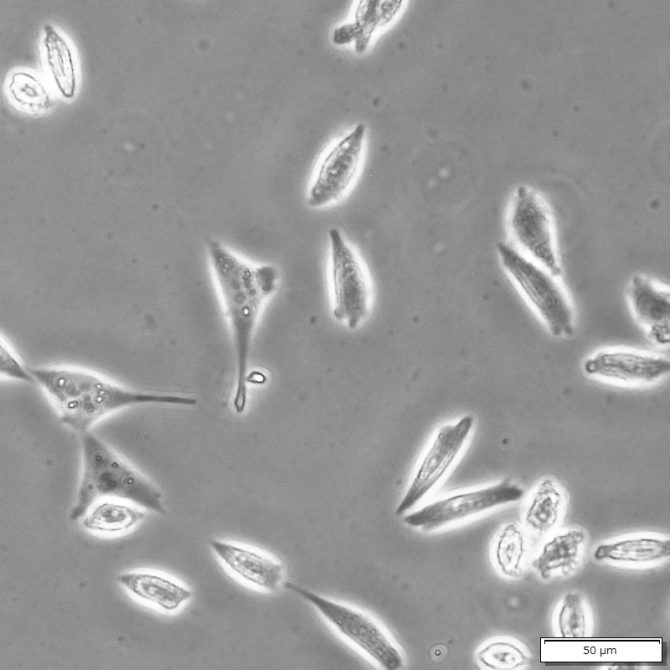
形が違う細胞が混じっているような…

緑色の蛍光を放つ細胞が混入していました
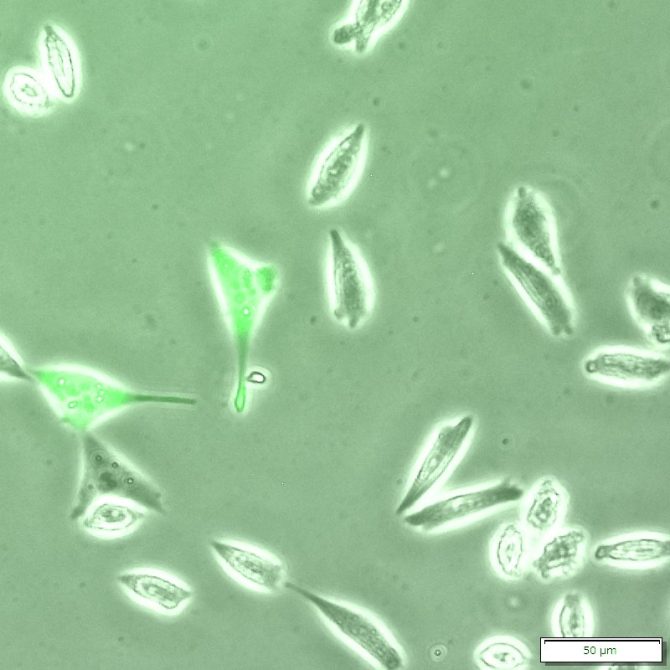
画像を重ねると混入した細胞がわかります
これも細胞培養における重大な事故です。クロスコンタミが起こる主な原因を5つ挙げます。
クロスコンタミの原因5選
(1) 複数の細胞株を同時に扱う
クリーンベンチ内で、2種類以上の異なる細胞を同時に持ち込んで操作することは非常に危険です。
「気をつければ大丈夫」と思っていても、ふとした時にディッシュやTフラスコのフタを取り違えたり、培地などの操作中に飛沫が入ったりします。
(2) 試薬・培地の共有ボトル使用
培地やトリプシンなどが入った試薬ボトルを、複数の細胞株で「共用(使い回し)」することです。
もし、一方の細胞を操作したピペットが誤ってボトルに触れ、そのボトルをもう一方の細胞Bに使えば、ボトル内の試薬を介して細胞が移動します。
(3) ピペットチップの交換忘れや誤った使用
細胞を懸濁したピペットチップを捨てずに、うっかりそのまま別のフラスコに入れてしまう、あるいはチップの交換を忘れて試薬を扱ってしまうケースです。
(4) ラベリング不備と取り違え
フラスコや凍結チューブへの記載が不十分(略称が似すぎている。書いていない。数字の「6」と「9」の取り違え)なために起こります。
特に凍結細胞を起こす際や、継代の忙しい時に、「どれがどっちだっけ?」と混乱し、結果として違う細胞として培養を続けてしまうケースです。
(5) エアロゾル(微小な飛沫)による移動
ピペッティング操作が激しいと、目に見えない微細な液滴(エアロゾル)が飛び散ります。
近くに蓋の開いた別のフラスコがあると、空気中を漂って隣のフラスコに着地し、混入することがあります。
このように、クロスコンタミネーションの原因は非常に身近であり、その多くは作業者自身の操作に起因します。
そのためトップレベルの研究者であっても、つい過信して「私の作業や管理は万全だ」と信じて疑わないことがあります。
こういった過信が、細胞培養の歴史を揺るがす重大な事件を引き起こすきっかけにもなります。
1960年代から70年代にかけて明らかになった衝撃の事実――それは、世界中で『異なる細胞』として研究されていたはずの多くの株が、実はすべて同じ細胞、すなわち『HeLa細胞』に入れ替わっていたという事件でした。
次にこの事件についてご紹介します。
世界規模で起こっていた(いる)クロスコンタミネーション
1951年に樹立されたHeLa細胞は、極めて高い増殖能を有することから、これまで多くの基礎研究に利用されてきました*1。
一方で、その旺盛な増殖能力ゆえに、ひとたび混入すると他の細胞株を急速に置き換えてしまうという特性も持ち合わせています。
その結果、研究者が別の細胞を使っているつもりで、実際はHeLaだったというケースが世界中で発生し、大規模な研究成果の信頼性が揺らぐ事態となりました*2。
クロスコンタミは我が国でも確認*3されており、該当する細胞株の分譲は基本的に停止されています*4。しかし場合によってはHeLa細胞の一つとして培養実験に利用することが可能となっています*5。
また、このようなクロスコンタミネーションは現在でも報告されており、HeLa 細胞に限らず他の細胞株でも別の細胞株が混入していた例も確認されています*6。
その影響は研究結果の再現性や信頼性に直結するため、細胞培養に関わるすべての研究者・技術者が「起こり得る前提」で管理・確認を徹底することが不可欠です。
*1:SCHERER WF, et al. Studies on the propagation in vitro of poliomyelitis viruses. IV. Viral multiplication in a stable strain of human malignant epithelial cells (strain HeLa) derived from an epidermoid carcinoma of the cervix. J Exp Med. 1953;97(5):695-710.
*2:Nelson-Rees WA, et al. Cross-contamination of cells in culture. Science. 1981;212(4493):446-452.
*3:Ogura H, et al. DETECTION OF HeLa CELL CONTAMINATION-PRESENCE OF HUMAN PAPILLOMA VIRUS 18 DNA AS HeLa MARKER IN JTC-3, OG AND OE CELL LINES, Jpn J Med Sci Biol. 1997; 50(4-5): 161-167.
*4:理化学研究所の細胞材料開発室で報告されたクロスコンタミが確認された細胞株一覧
*5:医薬基盤・健康・栄養研究所の細胞バンクに登録されたHeLa汚染細胞株の一例
*6:英語版Wikipediaに掲載されているクロスコンタミが確認された細胞株一覧
発生したらどうする?
微生物によるコンタミやクロスコンタミが発生した場合、基本的には細胞や培地、チップ、容器、関連試薬など、その細胞を扱ったものすべてを廃棄(滅菌処理)するのが最も安全な対応です。
一部を残して原因究明や再利用を試みたい気持ちもわかりますが、汚染源や感染経路が不明確な状態で汚染された器具類を残すことは、再発や他の培養への二次汚染リスクを高めることになります。
ディッシュやTフラスコへの廃棄方法としてはオートクレーブが最も簡単ですが、培地が外部に漏れ出さないように防水性のあるオートクレーブバッグを使用し、必要に応じて二重包装するなど、十分な漏洩対策を講じることが重要です。
なお、廃棄物処理に使用するオートクレーブは、通常の滅菌用途とは別系統で運用することが望まれます。
これは、高レベルの微生物汚染やクロスコンタミネーションの原因となるものが、オートクレーブ庫内やオートクレーブの排気系を介して残存・拡散するリスクを最小限に抑えるためです。

コンタミした器具類は適切に滅菌処理しましょう

汚染物は別にオートクレーブしましょう

オートクレーブ後がわかる標識を利用しましょう
廃棄によるコスト的・心理的な負担は避けられませんが、感染源や発生源となり得る物品を残すことによるリスクはそれ以上に大きく、ラボ全体の安全性や実験の信頼性を損なう可能性があります。
そのため、コンタミ発生時には「惜しまず廃棄する」ことが、結果として最も合理的なリスク管理となります。
またインキュベーターに対しては庫内の洗浄、アルコール噴霧と吹き上げ、専用消毒剤による処理に加え、乾熱滅菌や化学滅菌などをおこなった後、微生物によるコンタミのリスクを抑えるため、加湿水への微生物増殖抑制剤(例:銀イオンを活用した抗カビ製品)などの使用を推奨します。

銀イオンを活用した抗カビ製品の一例
抗カビ作用を持つ銀イオンを徐々に放出できる製品を推奨します
詳細は以下の記事をご参考ください。
参考1:【コンタミ】汚染の脅威から細胞を守るには
参考2:【コンタミ】細胞培養での除菌・殺菌・滅菌・無菌とは
参考3:【メンテ】コンタミ防止のためにあなたがとるべき対策
参考4:【メンテ】手軽にできるコンタミ防止対策
参考5:【コンタミ】なぜ銀イオンは微生物に効くのか?
まとめ
コンタミネーションは「避けられない失敗」ではなく、予防と管理によって大きく低減できるものであり、発生した場合には培養環境や操作を見直す重要なきっかけとなります。
- 細菌や真菌、酵母によるコンタミは急激に進行し、培地の色の変化や臭気によって気づきやすい。
一方でマイコプラズマによる汚染は変化に乏しいため汚染の判別が非常に困難。 - クロスコンタミは初期には目立った変化が無いものの、次第に細胞の特性が変化していくことで気づくことがある。
しかしほとんどの場合は気づかないため、定期的な検査(STR分析*1などDNAレベルでの解析)を推奨。 - インキュベーター由来のコンタミは清掃・点検・運用管理の不備により発生しやすく、日常管理の継続が不可欠である
これらの特性を正しく理解し、予防・監視・対応を徹底することで、細胞培養はより安全かつ安定したものとなることでしょう。
細胞は繊細で、環境に誠実に反応します。
その細胞と向き合う私たちの姿勢も、同じように丁寧であり続ける必要があるのだと思います。
*1:STR(Short Tandem Repeat:短鎖反復配列)分析とは、DNA中に存在する短い塩基配列の繰り返し数が個体ごとに異なるという特徴を利用し、細胞株の由来や同一性を確認する分析手法です。